Что на самом деле запрещает принцип Паули?
Когда-то в школе на химии нам рассказывали про устройство атома и схема распределения электронов по энергетическим уровням рисовалась квадратиками. В каждый квадратик можно было вписать две стрелочки. Причём, стрелочки эти должны были быть разнонаправленными.
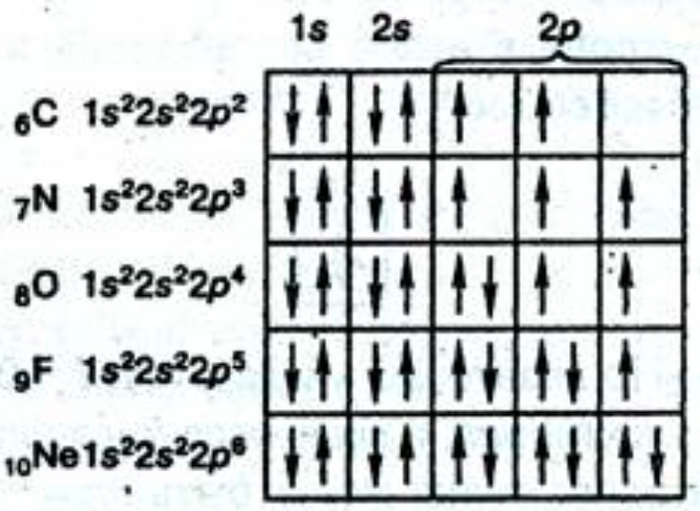
Вот эта схемка
А почему? Потому что работает принцип запрета Паули. Исходя из него нельзя нарисовать две одинаковых стрелочки в одной клетке. А что это значит с физической точки зрения? Никто не знал, что это значит. Причем, я почти уверен сейчас, что и преподаватель это не до конца осознавал. И важнейший принцип сводился к направлению стрелочек в клеточке.
Что же, вспомним формулировку принципа:
Принцип запрета Паули - это квантово-механический принцип, который гласит, что два или более тождественных фермиона (частицы с полуцелым спином) не могут одновременно находиться в одном и том же квантовом состоянии в квантовой системе.
Честно... Многим читателям ну совершенно ничего не понятно. Следовательно, и значение этого явления, которое куда более серьезно для всей физики, чем просто запрет нарисовать две одинаковых стрелочки, никому не понятно. Но в этом правиле есть ответ на один очень важный вопрос.
Итак, Вольфганг Паули первоначально сформулировал принцип исключения для электронов, но позже обобщил его и распространил на все фермионы. Поэтому, если при определённых условиях три электрона образуют составной фермион, то принцип Паули будет применим именно к составному фермиону. Протон и нейтрон являются типичными примерами сложных фермионов, к которым применим принцип Паули (состоящий из трех кварков). Но это всё опять голая теория и опять логика пошла не в ту степь. Слишком много академичности.
Именно из-за принципа Паули атомы занимают некоторый объём и не могут быть сильно сжаты, так как электроны одного и того же спина (↑↑) пространственно разделены отталкивающим обменным взаимодействием.
"Две одинаковых стрелочки" нельзя нарисовать в одном квадратике только потому, что электроны не могут расположиться так близко друг к другу.
Это обусловлено существованием взаимодействия между ними, которое приводит к взаимному отталкиванию. Так ведут себя однородные частицы с одинаковым спином.
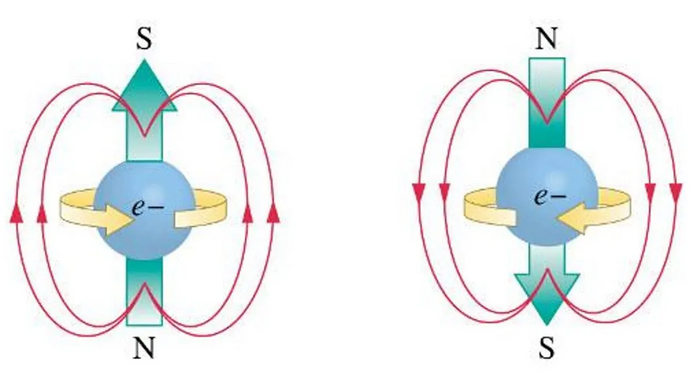
Спин - схема явления. Но на самом деле всё сложнее
Конечно физики меня сейчас будут сильно ругать (в глубокой теории спин не есть только лишь вращение), но проще всего тут представить спин механически. Спин это вращение вокруг своей оси. Если направления вращений частиц совпадают, то происходит нечто типа взаимного отталкивания и частицы мешают друг другу. Если направления вращения разные - то частицы могут занять некоторый единичный объем, а в случае строения атома оказаться на одном энергетическом уровне.
И самое главное тут - понять физический смысл принципа запрета Паули. К чему приводит существование такого явления?
К самым интересным последствиям. Именно по этой причине мы можем ходить по твердой поверхности.
Фактически для осязаемой материи правило можно перефразировать как:
Два твердых тела не могут находиться в одном и том же месте.
Но, если силы сжатия значительно больше, например, при гравитационном коллапсе звезды, то обменное отталкивание между электронами всё-таки может преодолеваться и фактически два тела при этом стремятся занять одно положение. В этом случае запрет Паули может быть нарушен, но это отдельная история.
⚡ Впрочем, буду рад, если вы подпишитесь на мой Telegram-канал.
Ещё я собрал три своих великолепных научпоп канала в удобную папку