РАК.Ингибирование микротрубочек препаратами многократного использования: мебендазол + иве + носкапин

Рисунок: Микротрубочки состоят из гетеродимера (гетеродимера), в котором α-тубулин и β-тубулин связаны как основная единица (①), и протофиламента, в котором гетеродимеры тубулина соединены в волокнистой форме.Это называется (②) , и 13 из них собираются вместе, образуя трубчатую структуру (диаметр 25 нм), которая становится микротрубочкой (③). Когда происходит деление клетки, ДНК реплицируется в клетке, а реплицированная ДНК (хромосома) притягивается микротрубочками (④) и делится в каждой клетке после деления (⑤). Мебендазол, ивермектин и носкапин связываются с тубулином и ингибируют процесс полимеризации/деполимеризации микротрубочек (⑥). В результате М-фаза клеточного деления останавливается и происходит гибель клеток (апоптоз). В дополнение к действию, ингибирующему микротрубочки, мебендазол обладает такими действиями, как ингибирование ангиогенеза, ингибирование пути Wnt/β-катенина и ингибирование сигнальной системы hedgehog. Ибермектин ингибирует путь Akt/mTOR и путь WNT-TCF, ингибирует р21-активируемую киназу (РАК-1), играющую центральную роль в сигнальной системе РАС, ингибирует ангиогенез и активирует противоопухолевый иммунитет. различными механизмами, такими как индукция иммуногенной клеточной гибели раковых клеток. Носкапин ингибирует факторы транскрипции, такие как NF-κB, рецептор эпидермального фактора роста (EGFR), фактор роста эндотелия сосудов (VEGF), индуцируемый гипоксией фактор-1α (HIF-1α) и белок P-сахара, участвующие в развитии множественной лекарственной устойчивости. влияние Следовательно, комбинация мебендазола, ивермектина и носкапина оказывает противоопухолевое действие за счет комплексного действия с помощью различных механизмов в дополнение к синергетическому действию, направленному на микротрубочки.
795) Ингибирование микротрубочек препаратами многократного применения: мебендазол + ивермектин + носкапин
[Лечение рака лекарствами многократного использования]
Терапия переменным током является типичным противораковым лекарственным средством для лечения рака молочной железы . Терапия АЦ представляет собой комбинацию двух типов противоопухолевых препаратов с разными механизмами действия, циклофосфамидаиадриамицина Циклофосфамид (эндоксан) был выпущен в Японии в 1962 году, а адриамицин (доксорубицин) был выпущен в Японии в 1975 году. Цисплатин , который используется для лечения многих видов рака, был одобрен в США и Канаде в 1978 году. Другими словами, противораковые препараты, которые использовались в течение почти 50 лет, по-прежнему используются в качестве основы для лечения рака. Если эти противораковые препараты обладают очень хорошим терапевтическим эффектом, вы можете быть уверены, что лекарств больше нет. Однако применение этих противоопухолевых препаратов может лишь продлить жизнь на несколько месяцев в случае распространенного рака. Как видите, есть много возможностей для разработки более эффективных противораковых препаратов, но трудно найти прорывное лекарство. Недавно были разработаны молекулярно-направленные препараты, воздействующие на клеточные рецепторы и вещества, передающие сигнал, но терапевтический эффект был не столь велик.
В последние годы внимание было сосредоточено на разработке противоопухолевых препаратов путем открытия новых показаний для уже используемых препаратов и их повторного использования в качестве препаратов для лечения других заболеваний .
Существующие лекарственные средства, применяемые для лечения заболеваний, отличных от рака, и вещества, которые были разработаны в качестве терапевтических средств для лечения заболеваний, отличных от рака, и прошли клинические испытания, но их эффективность не удалось доказать, и разработка была прекращена. о повторном использовании его в качестве лечебного средства от болезней.
Репозиционирование лекарств - это японский перевод слов « Перепозиционирование лекарств » или « Переназначение лекарств ». «Перепозиционирование» и «перепрофилирование» означают обновление позиции, позиции, цели и цели (пере-). Это означает повторное использование лекарств.
По сравнению с новой разработкой, она имеет то преимущество, что снижает затраты на разработку и сокращает период. В случае лекарственных средств для лечения рака, если противораковая активность обнаружена в экспериментах на животных (
, такие существующие лекарства и компоненты-кандидаты лекарствin vitroс использованиемin vivo
Недавно в базе данных были созданы вещества-кандидаты для лекарств, и с помощью компьютера выполняется поиск различной информации, такой как база данных клеточных рецепторов и структур веществ, передающих сигнал, и база данных паттернов генной экспрессии противоопухолевых препаратов ( in). ).
Термин «in silico» означает «в компьютере (кремниевом чипе)» и является термином, придуманным для in vitro (in vitro) и in vivo (in vivo) при полном использовании компьютеров. Это исследование, которое было проведено.
В Соединенных Штатах открыта для общественности база данных существующих лекарств, одобренных FDA (Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США), и веществ, которые не удалось разработать и которые хранятся в фармацевтических компаниях, а исследования по поиску новой эффективности различными методами в ходе выполнения.
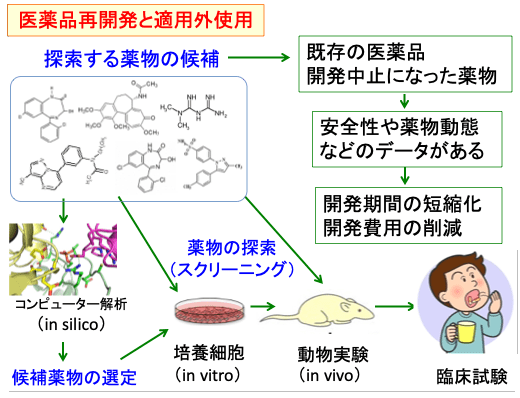
Рисунок: Противораковая активность лекарств или кандидатов в лекарства, разработанные для лечения заболеваний, отличных от рака, с помощью культивирования клеток (in vivo), экспериментов на животных (in vitro), компьютерного анализа (in silico) и т. д. Экран. Если обнаружена противораковая активность, доступны данные о безопасности и фармакокинетике, поэтому можно сократить период исследований и разработок, таких как клинические испытания, и снизить затраты на разработку. Если он уже использовался в качестве другого лечения, он может быть немедленно применен к лечению рака, если он не покрывается страховкой.
Из более чем 2000 препаратов, одобренных для лечения нераковых заболеваний, по крайней мере 235 доказали противоопухолевую активность in vitro, in vivo или клинически.
Из этих 235 препаратов 67 (29%) входят в Примерный перечень ВОЗ первой необходимости, 176 (75%) являются препаратами с истекшим сроком патента, а 133 (57%) имеют клинические данные для онкологических больных. Четыре типа (талидомид, общая транс-ретиноевая кислота, золедроновая кислота и нестероидные противовоспалительные препараты) уже имеют рекомендации по их использованию при лечении рака.
Другие многоразовые препараты, которые, как сообщалось, эффективны при лечении рака в рандомизированных клинических испытаниях, включают циметидин (колоректальный рак), прогестерон (рак молочной железы) и итраконазол (рак легких).
(Источник: Перепрофилирование нераковых препаратов в онкологии - Сколько существует лекарств? BioRxiv. 2017: 197434.)
Если вы попытаетесь использовать такой препарат для лечения рака, вы не сможете прописать его в Японии, если у вас нет страховки. Например, при назначении метформина со страховкой требуется название «диабет». Если у вас нет застрахованного заболевания, вы не сможете использовать его в медицинском учреждении со страховкой, даже если доказана его эффективность против рака.
Однако, если это медицинское учреждение с бесплатным медицинским обслуживанием, возможны рецепты, не покрываемые страховкой. Врачи могут назначать лекарства не по прямому назначению, если они являются бесплатным лечением (самофинансируемое лечение).
Есть много примеров нестрахового использования, которые полезны при лечении таких видов рака, и такие лекарства используются в альтернативной медицине для лечения рака.
[Работают ли средства от паразитов при раке? ]
Многие заболевания, такие как болезни сердца, болезни головного мозга и нарушения обмена веществ, вызваны ухудшением или потерей функций органов и тканей.
Рак, с другой стороны, вызван развитием новых тканей, состоящих из аномальных клеточных масс. Раковая ткань представляет собой массу клеток с аномальной пролиферативной способностью, но она объединяет нормальные стромальные клетки (фибробласты, воспалительные клетки и т. д.) и кровеносные сосуды, образуя новый агрегат, который можно назвать единой тканью. Он обладает способностью размножаться автономно, распространяется по всему телу путем инфильтрации и метастазирования и размножается бесконечно, пока наше тело-хозяин не умрет.
Эти свойства аналогичны инфекционным заболеваниям, таким как паразиты и бактерии.
Другими словами, рак имеет свойство паразитировать в организме, как паразит, и разрушать нормальный организм .
Непонятно почему, но известно много примеров лекарств, используемых для лечения паразитов, которые также эффективны против рака.
Поскольку они имеют мало побочных эффектов, очень безопасны и относительно недороги, была указана возможность лечения рака путем комбинирования нескольких этих средств для лечения паразитов.
Мебендазол - противогельминтное средство широкого действия на основе бензимидазола. Он широко действует на многих паразитов, таких как нематоды, ленточные черви и круглые черви. Сообщалось о сильной противораковой активности в нескольких экспериментальных системах, таких как культивирование клеток (in vitro), эксперименты на животных (in vivo) и компьютерный анализ (in silico).
Было показано, что в качестве механизма действия для уничтожения паразитов мебендазол ингибирует полимеризацию тубулина и ингибирует действие микротрубочек, которые играют важную роль в делении клеток .
Паклитаксел (торговое название; таксол) и винкристин являются примерами ингибирования микротрубочек. Паклитаксел стабилизирует микротрубочки, способствуя полимеризации тубулина, и ингибирует деление раковых клеток. Микротрубочки образуются из димеров α- и β-тубулина, из которых таксол связывается с β-тубулином и способствует его полимеризации, проявляя тем самым противораковую активность.
С другой стороны, мебендазол связывается с тубулином и ингибирует полимеризацию микротрубочек . Мебендазол связывается с колхицинсвязывающим доменом тубулина.
Мебендазол также оказывает противораковое действие посредством различных механизмов, таких как ингибирование ангиогенеза, ингибирование пути Wnt/β-катенина и ингибирование сигнальной системы hedgehog. (Рисунок ниже)

Рисунок: ДНК (хромосомы), реплицируемая во время клеточного деления, делится на клетки микротрубочками (①). Микротрубочки состоят из гетеродимера, в котором α-тубулин и β-тубулин связаны как основная единица Микротрубочки имеют структуру (25 нм в диаметре). Мебендазол связывается с тубулином, ингибирует полимеризацию микротрубочек, останавливает М-фазу клеточного деления и вызывает апоптоз (②). Когда фактор роста эндотелия сосудов (VEGF) связывается с рецептором фактора роста эндотелия сосудов-2 (VEGFR-2), VEGFR-2 образует димер и представляет собой остаток тирозина, присутствующий в домене тирозинкиназы.Запускается самофосфорилирование, внутриклеточный сигнал активируется система трансдукции, стимулируется пролиферация эндотелиальных клеток сосудов и ангиогенез, а также ангиогенез (③). Мебендазол блокирует активацию VEGFR-2 и ингибирует ангиогенез (④). Когда Wnt связывается с рецептором Frizzled и LRP5/6 и сигнал Wnt активируется, β-катенин увеличивается в цитоплазме и транслоцируется в ядро для связывания с фактором транскрипции TCF, а β-катенин/ активирует транскрипцию мишени TCF. генов (c-myc, циклин D1 и др.) и способствует пролиферации клеток (⑤). Мебендазол ингибирует TNIK (киназу, взаимодействующую с Traf2 и Nck), киназу, активирующую TCF, и ингибирует транскрипционную активность TCF (⑥). Таким образом, мебендазол ингибирует рост раковых клеток и вызывает гибель клеток с помощью различных механизмов.
[Ивермектин проявляет противораковую активность с помощью различных механизмов]
Ивермектин был получен из авермектинов, выделенных из ферментированного продукта актиномицета Streptomyces avermitilis , выделенного из почвы. В Японии он покрывается страховкой для лечения кишечных фекальных нематодозов и чесотки. Ивермектин является панацеей от филяриатоза,
который распространен в Латинской Америке и Африке, в Нигерии и Эфиопии . Нитевидный червь, также известный как онхоцеркоз или речная слепота, вызывает нарушения зрения, включая сильный зуд, обезображивающие изменения кожи и необратимую слепоту. Кроме того, он эффективен при многих видах паразитарных заболеваний, таких как лимфатический филяриатоз, и широко используется в качестве терапевтического препарата при паразитарных заболеваниях у животных и человека.
Ивермектин избирательно и с высоким сродством связывается с глутаматергическими хлоридными (Cl) каналами, присутствующими в нервных и мышечных клетках беспозвоночных . Результатом является хлорид (повышенная проницаемость клеточной мембраны для Cl, что приводит к гиперполяризации нервных или мышечных клеток, что приводит к параличу и гибели паразита. У млекопитающих присутствие Cl-каналов, управляемых глутаматом, не сообщалось, можно сказать, что безопасность чрезвычайно
высока.Таким образом, безопасность ибермектина очень высока, и иммунный ответ, вызванный процессом смерти паразита против зараженного паразитом человека, говорит, что есть несколько побочных эффектов, кроме симптомов вызванные воспалительной реакцией.
Кроме того, многочисленные доклинические исследования подтвердили противораковые эффекты.
В экспериментах с использованием культивируемых клеток сообщалось о противоопухолевых эффектах при многих типах рака, таких как рак молочной железы, рак яичников, рак предстательной железы, рак головы и шеи, рак толстой кишки, рак поджелудочной железы и злокачественная меланома. Клинически было показано, что он оказывает противоопухолевое действие при уровнях в крови, которые могут быть достигнуты человеком.
Сообщалось, что он не только подавляет пролиферацию и индуцирует апоптоз, но также ингибирует ангиогенез. Противоопухолевый эффект был также подтвержден в экспериментах на животных.
В качестве механизма противоракового действия ивермектина сообщалось об ингибировании митохондриального дыхания, индукции окислительного стресса, ингибировании пути Akt/mTOR, ингибировании пути WNT-TCF, ингибировании PAK-1, ингибировании ангиогенеза и т. д. Есть следующие обзорные статьи.
Многоцелевое лекарственное средство ивермектин: от противопаразитарного средства к репозиционированному лекарству от рака Am J Cancer Res., 2018; 8 (2): 317-331.
[Аннотация]
Репозиционирование лекарств активно изучается как одно из средств открытия и разработки противоопухолевых препаратов. С помощью этого метода разработки лекарств в существующих лекарствах были обнаружены новые применимые заболевания. Ивермектин представляет собой соединение группы авермектинов, типа 16-членного макроциклического лактона, открытого в 1967 г., и было использовано FDA (США) в 1987 г. для применения человеком. Одобрено Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов).
Ивермектин используется большим количеством пациентов во всем мире, и его клиническая безопасность чрезвычайно высока. В этом обзоре обобщены данные in vitro и in vivo о том, что ивермектин оказывает противоопухолевое действие с помощью различных механизмов при многих типах рака.
Ивермектин представляет собой белок с множественной лекарственной устойчивостью (MDR), Akt/mTOR и путь WNT-TCF, пуринергический рецептор, белок PAK-1, связанные с раком эпигенетические дерегуляторные факторы, такие как SIN3A и SIN3B, активность РНК-хеликазы.Он действует на несколько мишеней, такие как рецепторы хлоридных каналов, особенно нацеленные на раковые клетки с характеристиками раковых стволовых клеток.
Важно отметить, что противоопухолевая активность ивермектина in vitro и in vivo достигается при клинически достижимых концентрациях, что основано на исследованиях фармакокинетики человека, проведенных на здоровых людях и пациентах, инфицированных паразитами . Таким образом, имеющаяся информация об ивермектине позволяет быстро перейти к клиническим испытаниям на онкологических больных.
Известно, что противоопухолевые агенты с одной мишенью и высокой селективностью имеют тот недостаток, что раковые клетки, приобретшие резистентность, появляются быстро. Поэтому было указано, что для цели важно разработать противораковый препарат, который оказывает противораковое действие с помощью различных механизмов.
В связи с этим ибермектин представляет собой связанный с раком эпигенетический дерегуляторный фактор, такой как белок с множественной лекарственной устойчивостью (MDR), пути Akt/mTOR и WNT-TCF, пуринергические рецепторы, белок PAK-1, SIN3A и SIN3B. , Модулирует несколько мишеней, таких как РНК-хеликазная активность, а также стимулирует рецепторы хлоридных каналов, что приводит к клеточной гиперполяризации и подавляет экспрессию генов, поддерживающих свойства раковых стволовых клеток, по крайней мере, при раке молочной железы.
Что еще более важно, противоопухолевая активность ивермектина in vitro и in vivo должна быть достигнута в клинически достижимых концентрациях, основанных на фармакокинетических исследованиях человека, проведенных на здоровых пациентах и пациентах с паразитами.
Таким образом, имеется достаточно доказательств для начала клинических испытаний ивермектина в качестве средства для лечения рака.
[Ивермектин ингибирует микротрубочки]
Сообщалось, что ивермектин связывается с тубулином и ингибирует функцию микротрубочек . Имеются следующие отчеты.
Ивермектин проявляет мощную антимитотическую активность Vet Parasitol. 2016 Aug 15; 226: 1-4.
Резюме:
Ивермектин применяют в качестве антигельминтного препарата для сельскохозяйственных животных, домашних животных и человека. Считается, что основным участком действия ивермектина является глутамат-зависимый хлоридный канал. Однако недавно было сообщено, что ивермектин и тубулин нематоды взаимодействуют непосредственно с микромолярным сродством . Здесь мы сообщаем, что ивермектин также взаимодействует с тубулином млекопитающих.
Чтобы проверить эту возможность, мы использовали анализ полимеризации тубулина и обнаружили, что ивермектин увеличивает степень полимеризации тубулина млекопитающих.
Кроме того, воздействие ивермектина на клетки HeLa стабилизировало тубулин млекопитающих против низкотемпературных реакций деполимеризации тубулина и предотвращало репликацию клеток HeLa in vitro. Однако ингибирование клеточного деления ивермектином в клетках HeLa было обратимым.
Экспериментальные данные свидетельствуют о том, что ивермектин связывался с микротрубочками млекопитающих и стабилизировался ивермектином в микромолярных концентрациях .
Поэтому было высказано предположение, что ивермектин может вызывать гибель клеток, влияя на динамику полимеризации и деполимеризации тубулина. Учитывая, что ивермектин уже был одобрен для использования у людей, его разработка в качестве ингибитора митоза является потенциально привлекательным вариантом.
Ивермектин связывается с тубулинами Haemonchus contortus и способствует стабильности микротрубочек Int J Parasitol. 2015 Aug; 45 (9-10): 647-54 ..
[Выдержка из аннотации]
Haemonchus contorn является нематодой домашнего скота и вызывает серьезные заболевания и смерть. Ивермектин, противопаразитарное средство, воздействующее на глутаматзависимые хлорные каналы, широко используется у людей, домашнего скота, домашних животных и в сельском хозяйстве. Тубулин/микротрубочки являются важными мишенями для многих антимитотических препаратов, используемых при лечении паразитов и рака. Мы сообщаем, что воздействие ивермектина увеличивало скорость и степень полимеризации рекомбинантных α- и β-тубулинов у Haemonchus contornata и защищало α- и β-тубулины паразита от ограниченного протеолиза трипсином.
Ивермектин и мономер тубулина связываются непосредственно с низкой микромолярной аффинностью .
Было показано, что ивермектин и таксол конкурируют за связывание с тубулином, предполагая, что ивермектин взаимодействует как с карманами связывания таксола тубулина, так и у млекопитающих.
Таким образом, наши данные показывают, что ивермектин может связываться с микротрубочками и стабилизировать их (т. е. изменять равновесие полимеризации тубулина), что может приводить к остановке митоза. Результаты этого эксперимента расширили спектр известных фармакологических эффектов ивермектина и выявили его потенциал в качестве антимитотического агента.
Другими словами, ивермектин оказывает противоопухолевое действие с помощью различных механизмов, и можно сказать, что микротрубочки являются одной из мишеней ивермектина.

Рисунок: Ивермектин используется для лечения многих паразитарных заболеваний, таких как фекальные нематоды, нитевидные черви и чесотка. Ибермектин ингибирует путь Akt/mTOR и путь WNT-TCF, ингибирует р21-активируемую киназу (РАК-1), играющую центральную роль в сигнальной системе РАС, ингибирует ангиогенез, ингибирует микротрубочки и раковые клетки, проявляет противоопухолевую активность за счет различные механизмы, такие как индукция иммуногенной гибели клеток.
[Микротрубочки необходимы для клеточного деления]
Микротрубочки представляют собой высокодинамичные структуры, состоящие из гетеродимеров (гетеродимеров) α-тубулина и β-тубулина , они участвуют в миграции клеток и внутриклеточно, участвуют в транспорте и необходимы для клеточного деления. Микротрубочки стали важной мишенью для разработки противоопухолевых препаратов, поскольку они играют важную роль в делении клеток в фазе G2/M.
Известно, что различные природные молекулы, такие как алкалоид барвинка, паклитаксел, комбретастатин и колхицин, ингибируют функцию микротрубочек.
Некоторые из этих агентов, нацеленных на микротрубочки, ингибируют полимеризацию тубулина, в то время как другие ингибируют деполимеризацию тубулина.В основном они связываются с тубулином, чтобы осуществить реакцию полимеризации и реакцию деполимеризации тубулина.Ингибируют. Сообщалось о сайте связывания ингибитора микротрубочек тубулина.

Рисунок: Известные сайты связывания агентов, нацеленных на микротрубочки, на тубулине. (Источник: Trends Cell Biol. 2018; 28: 776-792.)
Препараты, действующие на микротрубочки, такие как производные таксола и алкалоиды барвинка, являются мощными противоопухолевыми препаратами, используемыми при различных видах рака. Однако эти препараты токсичны, включая периферическую невропатию, желудочно-кишечную токсичность, миелосупрессию и иммуносупрессию.
С другой стороны, в мебендазоле, ибермектине и носкапине носкапин ингибирует функцию микротрубочек, но периферическая невропатия, такая как другие ингибиторы микротрубочек (паклитаксел, доцетаксел, алкалоид барвинка и т. д.), желудочно-кишечные расстройства, миелосупрессия и т. д. побочные эффекты.
Ингибирующий эффект носкапина на микротрубочки был объяснен в прошлый раз ( эпизод 794 ).
Странно, что у него нет таких побочных эффектов, как у других противоопухолевых препаратов, если он подавляет функцию микротрубочек, необходимых для деления клеток. Было указано, что причина этого заключается в том, что сайт-мишень для ингибирования микротрубочек отличается от паклитаксела, доцетаксела и винорелбина.
Комбинация мебендазол + ивермектин + носкапин синергически угнетает функцию микротрубочек. Эти три типа являются хорошо известными препаратами для лечения рака с помощью многоразовых лекарств. Он проявляет противоопухолевую активность посредством многих механизмов, отличных от ингибирования микротрубочек. Более того, побочные эффекты крайне незначительны.
Кроме того, эффективны итраконазол , противогрибковый препарат, повышающий уровень мебендазола и ивермектина в крови, и пищевая сода , повышающая внутриклеточное поглощение носкапина .
Итраконазол сам по себе оказывает противоопухолевое действие по различным механизмам. ( см. серию 727 )

Рисунок: Холестерин в крови (липопротеин низкой плотности (ЛПНП)-холестерин) связывается с рецептором ЛПНП в покрытых клатрином ямках клеточной мембраны и перемещается в клетку посредством эндоцитоза (①). После этого эндосомы созревают (②) и сливаются с лизосомами (③). В лизосомах свободный холестерин высвобождается в цитоплазму лизосомальными ферментами и транспортируется в органеллы (эндоплазматический ретикулум, аппарат Гольджи, митохондрии) и плазматическую мембрану (④). Диссоциированный рецептор возвращается на клеточную мембрану и используется повторно (⑤). Итраконазол ингибирует внутриклеточный транспорт холестерина из лизосом в цитоплазму (⑥) и, как следствие, угнетает сигнальную систему mTOR и ангиогенез, а также подавляет рост раковых клеток (⑦).
В качестве альтернативного лечения рака с небольшим количеством побочных эффектов стоит попробовать комбинацию мебендазол + ивермектин + носкапин + итраконазол + пищевая сода. Мы подтвердили противоопухолевый эффект, фактически применив его при прогрессирующем раке. Редко испытывают серьезные побочные эффекты.
795)再利用医薬品による微小管阻害:メベンダゾール+イベルメクチン+ノスカピン
...
blog.goo.ne.jp