Зарождение жизни (Заметка)
Зарождение жизни
Зарождение жизни на любой Земле, возможно при наличии белка. Белок образуется при электрическом разряде. Это доказали следующим опытом.
Абиотический синтез биомономеров
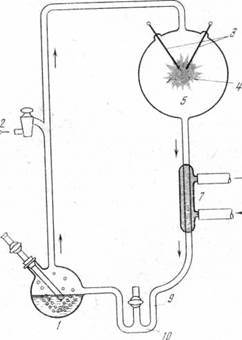
Синтез аминокислот при действии электрических разрядов в газовой смеси, имитирующей возможный состав примитивной земной атмосферы, был осуществлен еще в 1953 г в широко известных в настоящее время опытах Миллера. Использованный для этой цели прибор Миллера изображён на рис 1. Он состоит из большого круглого сосуда, в котором находится исходная смесь газов и в котором производится электрический разряд, а также малой колбы с кипящей водой - в ней скапливаются получающиеся продукты.
При действии искрового или тихого разряда на смесь СН4, NH3, H2 и паров воды при постоянной (в течение недели) циркуляции смеси в малой колбе были обнаружены глицин, α-аланин, α -аминомасляная и α -аминоиз масляная кислоты, β-аланин, аспарагиновая и глутаминовая кислоты, саркозин и N-СН2-аланин. Промежуточными продуктами этой реакции являлись альдегиды HCN.
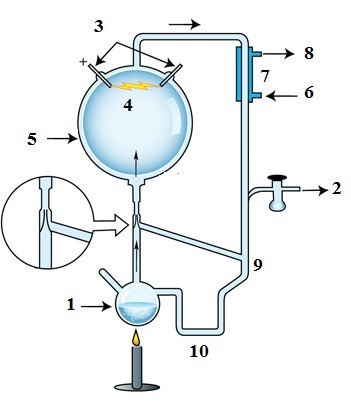
Рис.1. Прибор Миллера для синтеза органических соединений в восстановительной атмосфере под действием искровых разрядов
1 - колба с кипящей водой; 2 - к вакуумному насосу; 3 - электроды; 4 - искровой разряд; 5 - смесь газов (СН4,NH3, Н2О, Н2); 6 - выход воды из холодильника; 7 - холодильник; 8 - подача воды в холодильник; 9 - вода, содержащая органические соединения; 10 - ловушка
Данные Миллера были подтверждены в работе Т. Е. Павловской и А. Г. Пасынского, в которой применялась несколько другая аппаратура, а избыточное количество водорода заменялось на СО. В последующих работах указанных авторов было обосновано положение, согласно которому любая реакция, приводящая к образованию альдегидов и HCN, обязательна должна была способствовать накоплению α -аминокислот в гидросфере первичной Земли.
Эбельсон, используя более сложную исходную смесь газов, включающую наряду с СН4, NH3 и Н2О также) СО, СО2 и N2, получил аналогичную Миллеру смесь аминокислот. Оро, используя С2- и С3-углеводороды и концентрированный NH4OH, дополнил указанный список синтезированных в искровом разряде аминокислот лейцином изолейцином и валином. Гроссенбахер, пропуская искровой разряд в специально сконструированном приборе в течение 100 - 200 час. через смесь NH3, CH4 и Н2, получил в водном; растворе смесь аминокислот (соотношение в молях): аспарагиновая кислота - 2, треонин - 4, серии-14, глицин- 16, аланин-14, лизин - 4, лейцин - 2, изолейцин - 2 и глутаминовая кислота - 1. Кроме того, он обнаружил пептиды, состоящие из глицина и аланина (5:1), а также глицина и изолейцина. К концу опыта продукты полимеризации аминокислот выделялись из раствора в виде мелких многомолекулярных сфер или капель.
Менее многочисленны исследования по синтезу аминокислот при воздействии на смесь примитивных газов ионизирующими излучениями. Здесь можно назвать опыты Дозе и Раевского, обнаруживших образование кислых и нейтральных аминокислот при действии рентгеновых лучей на газовую смесь СН4, NH3, H2, CO2, N2 и Н2О. При облучении β-лучами от линейного ускорителя (2 Мэв) растворов ацетата аммония Гассельстромом, Генри и Мурром были получены глицин и аспарагиновая кислота, а при Х-облучении 60Со (5*108 р) твердого карбоната аммония Пашке, Чанг и Янг доказали образование глицина и аланина. Пальм и Кальвин, действуя на смесь метана, аммиака, водорода и паров воды пучком быстрых электронов (5 Мэв при дозе 1010 эрг), синтезировали глицин и аспарагиновую кислоту.
Образование аминокислот при простом нагревании исходных растворов было впервые обнаружено Фоксом, Джонсоном и Вегодским. Оро с сотрудниками показал, что ряд аминокислот (глицин, аланин, серии, аспарагиновая кислота, треонин) получается просто при нагревании в течение 40-60 час. водных смесей формальдегида и гидроксиламина при 80-100° С или даже при более низких температурах. Аналогичные результаты были получены Левом, Рисом и Маркхемом, которые нагревали 1,5 М водный раствор NH3 и HCN при 90° в течение 18 час. и обнаружили при этом значительное количество аминокислот, частично входящих в пептиды и освобождающихся после гидролиза продуктов реакции (в том числе, кроме глицина, аланина и аспарагиновой кислоты, они получили также лейцин, изолейцин, серии, треонин и глутаминовую кислоту).
Но, конечно, основное значение для первичного абиогенного синтеза органических веществ имела все же энергия коротковолновых ультрафиолетовых лучей, легко достигавшая земной поверхности вследствие отсутствия в доактуалистическую эпоху озонового экрана. Синтез аминокислот и других органических соединений при экспериментальной имитации такого рода условий особенно широко представлен сейчас в мировой литературе.
Т. Е. Павловская и А. Г. Пасынский при облучении водных растворов, содержащих 2,5% формальдегида и до 1,5% хлористого или азотнокислого аммония, ультрафиолетовыми лучами от лампы ПРК-2 в течение 20 час. установили образование следующих аминокислот: серина, глицина, глутаминовой кислоты, аланина, валина, фенилаланина и основных аминокислот - лизина, орнитина и аргинина.
В присутствии адсорбентов (бентонита, каолинита, лимонита и оптического кварца) были найдены те же аминокислоты (за исключением основных) и, кроме того, изолейцин. В последующей работе было показано образование треонина, а при замене формальдегида ацетальдегидом - аргинина и тирозина. Аналогичные результаты были получены другими авторами при облучении коротковолновым ультрафиолетовым светом смеси примитивных газов и их ближайших производных. Нужно отметить, что как при электрических разрядах, так и при освещении ультрафиолетовыми лучами в использованных для синтеза примитивных смесях образуются не только аминокислоты, но также органические кислоты и альдегиды, амины и амиды, в частности мочивина. Вместе с тем в этих условиях происходит полимеризция мономерных молекул, приводящая к образованию более сложных соединений.
Абиотический синтез полимеров
Следующим за образованием мономеров шагом эволюции на пути к возникновению жизни являлось их объединение в полимеры, в частности в соединения, аналогичные белкам и нуклеиновым кислотам, играющим исключительно важную роль в организации живых существ.
Принципиальная возможность такой далеко идущей абиогенной полимеризации органических веществ подтверждается рядом опытов, где в качестве мономеров использовались в первую очередь аминокислоты и родственные им соединения.
Здесь прежде всего нужно упомянуть об исследованиях Акабюри, который еще в 1955 г. указывал на возможность в условиях примитивной Земли абиогенного синтеза протобелков (т. е. аминокислотных полимеров со случайным расположением аминокислотных остатков в полипептидной цепи). Вскоре он доказал эту возможность экспериментально, получая из формальдегида, аммиака и HCN аминоацетонитрил, поликонденсат которого адсорбировался на каолине с образованием полиглицина. Затем в полиглицин можно вводить боковые Цепи путем реакции с альдегидами или с ненасыщенными углеводородами. Таким путем Акабюри удалось получить полиглицин и его аналоги с молекулярным весом приблизительно равным 15 000.
Фокс и его сотрудники, имитируя вулканические условия, подвергали смесь 18 аминокислот нагреванию при 170° С на куске лавы в течение 6 час. Для того чтобы расплавить смесь до ее обугливания, бралось избыточное количество дикарбоновых аминокислот. В других случаях нагревание осуществлялось в присутствии полифосфатов, что позволяло снизить температуру нагревания до 100° С.
При таком температурном воздействии образуется янтарного цвета полимер с молекулярным весом в несколько тысяч (от 5 000 до 10 000), содержащий все взятые в опыт типичные для белка аминокислоты (потерявшие, однако, свою оптическую активность). Этот полимер был назван Фоксом протеиноидом за его сходство по ряду признаков с белками.
При дальнейших исследованиях были выявлены два очень интересных свойства протеиноидов: во-первых, то, что они обладают известной внутримолекулярной упорядоченностью, повторяющейся последовательностью аминокислотных остатков, и, во-вторых, имеют хотя и слабую, но вполне экспериментально обнаруживаемую ферментативную активность (катализ гидролиза, декарбоксилирования, аминирования и дезамннирования).
Из многочисленных работ по синтезу полипептидов в водной среде следует назвать следующие: поликонденсацию глицина при его нагревании в водном растворе аммония, при γ-облучении; ацетилглицин при термальной обработке растворов цианистого аммония, при нагревании смеси HCN, NH3, при полимеризации аминоацетонитрила, цианамида и дицианамида.
Очень важным вопросом при синтезе полипептидов и белковоподобных соединений является та последовательность, с которой аминокислотные остатки связываются между собой в полипептидные цепи. При современном биологическом синтезе белков эта характерная для каждого индивидуального белка последовательность (первичная структура) определяется нуклеиновым кодом, но, как указывалось выше, уже при термальном синтезе Фокса, в отсутствие нуклеиновых кислот создался некоторый постоянный порядок соседствования аминокислот.
Штейнман присоединял первую в ряду аминокислоту к гранулам высокомолекулярного полимера (хлорметилированного полистирола) и таким образом получал смолу с присоединенной к ней одной аминокислотой. Затем он исследовал относительную эффективность присоединения к ней ряда других аминокислот с незащищенной аминогруппой.
Экспериментально определяя выходы различных дипептидов, Штейнман сопоставлял эти результаты с частотой аминокислотных пар, определенных по «Атласу белковых структур» в современных белках, и обнаружил значительное совпадение. Кальвин в своей книге «Химическая эволюция» дает модель системы воспроизведения полипептида без матрицы, на основании контроля со стороны растущего конца. Интересно сопоставить эти высказывания Кальвина с замечательным синтезом полипептида (грамицидина С), осуществленным Липманном.
В более сложных и довольно трудновоспроизводимых в природе условиях были синтезированы и полимеры нуклеотидов, образующие цепочки, аналогичные молекулам нуклеиновых кислот современных организмов.
Замечательные работы Корнберга и другие показали возможность синтеза нуклеиновых кислот in vitro. Однако эти биосинтезы могут проходить только в присутствии соответствующего специфического фермента, и поэтому они не могут служить моделью для абиогенных процессов на примитивной Земле.
Некоторая вероятность такого синтеза была впервые намечена Шраммом в его работах с полифосфорным эфиром. В дальнейшем было показано, что цитидинфосфат может конденсироваться в олигонуклеотиды с помощью полифосфорной кислоты. В модельных опытах, более приближающихся к условиям первичной Земли, была показана способность карбодиимида стимулировать образование ди- и тринуклеотидов из смеси нуклеозидов и нуклеотидов в разведенных водных растворах (Оргель и сотр.).
Особую роль в процессах первичной полимеризации играют, по-видимому, фосфорные соединения. При температурах около 300° С и выше фосфорная кислота полностью конденсируется с образованием полифосфатов. Поэтому на поверхности примитивной Земли, с ее широко идущим локальным разогревом, полифосфаты и их органические соединения должны были образовываться в довольно широком масштабе.
В настоящее время неорганические полифосфаты обнаружены в значительных количествах у низших организмов: у бактерий, водорослей, грибов и некоторых простейших. Это линейные полимеры ортофосфорной кислоты с молекулярным весом 30 000-100 000. Из ряда объектов выделены также циклические тримета- и тетраметафосфаты.
Как было показано Н. С. Кулаевым и другими, неорганические полифосфаты играют существенную роль в энергетическом обмене низших организмов в противоположность высокоорганизованным живым существам, для которых они не являются характерными.
Все это позволяет думать, что на заре возникновения жизни на Земле неорганические полифосфаты вполне могли участвовать в образовании простейших механизмов сопряжения энергодающих и энергопотребляющих реакций, т. е. играть ту роль в предбиологическом и раннем биологическом обмене, которая сейчас осуществляется аденозинтрифосфорной кислотой.
Поннамперума, Саган и Маринер использовали этилметафосфат для модельных опытов по синтезу нуклеотидных компонентов. При этом необходимым источником энергии им служил ультрафиолетовый свет с длиной волны 2400-2900 А, который был вполне доступен примитивной земной поверхности. Синтезы велись в водных растворах аденина, аденозина, адениловой кислоты, рибозы и этилметафосфата. Смеси освещались ультрафиолетовым светом с длиной волны 2537 А при 40°С. При этом было установлено превращение аденина в аденозин, аденозина в аденозинмонофосфат (АМФ), АМФ в аденозиндифосфат (АДФ) и наконец АДФ в аденозинтрифосфат (АТФ). Таким образом, была доказана возможность абиотического синтеза в условиях доактуалистической земной поверхности аденозинтрифосфорной кислоты - этой основной «энергетической валюты» современных высших организмов.
Итак, широко развернувшиеся в настоящее время модельные опыты по абиотическому синтезу органических веществ в условиях, имитирующих примордиальные земные условия, позволяют нам с известной долей вероятности представить себе последовательный ход химической эволюции от простейших углеродистых соединений к высокополимерным веществам, из которых образовались те «организованные элементы» или примитивные организмы, остатки которых мы обнаруживаем в отложениях земной коры.
На этом этапе развития материи и произошел на нашей планете переход от химической эволюции к биологической, когда из гомогенного раствора органических веществ обособились индивидуальные целостные системы - пробионты, а затем и первичные живые существа.
***
Зарождение жизни (Заметка)
https://cyberpedia.su/19x594a.html
[Spoiler (click to open)]#белок #абиотический #синтез #Миллер #зарождение #жизни #Левашов
белок, абиотический, синтез, Миллер, зарождение, жизни, Левашов