США одобрили цефтобипрол сразу по трем показаниям
Управление по контролю качества пищевых продуктов и лекарственных средств США (FDA) одобрило цефалоспорин пятого поколения к применению по трем разным показаниям, говорится в пресс-релизе организации.
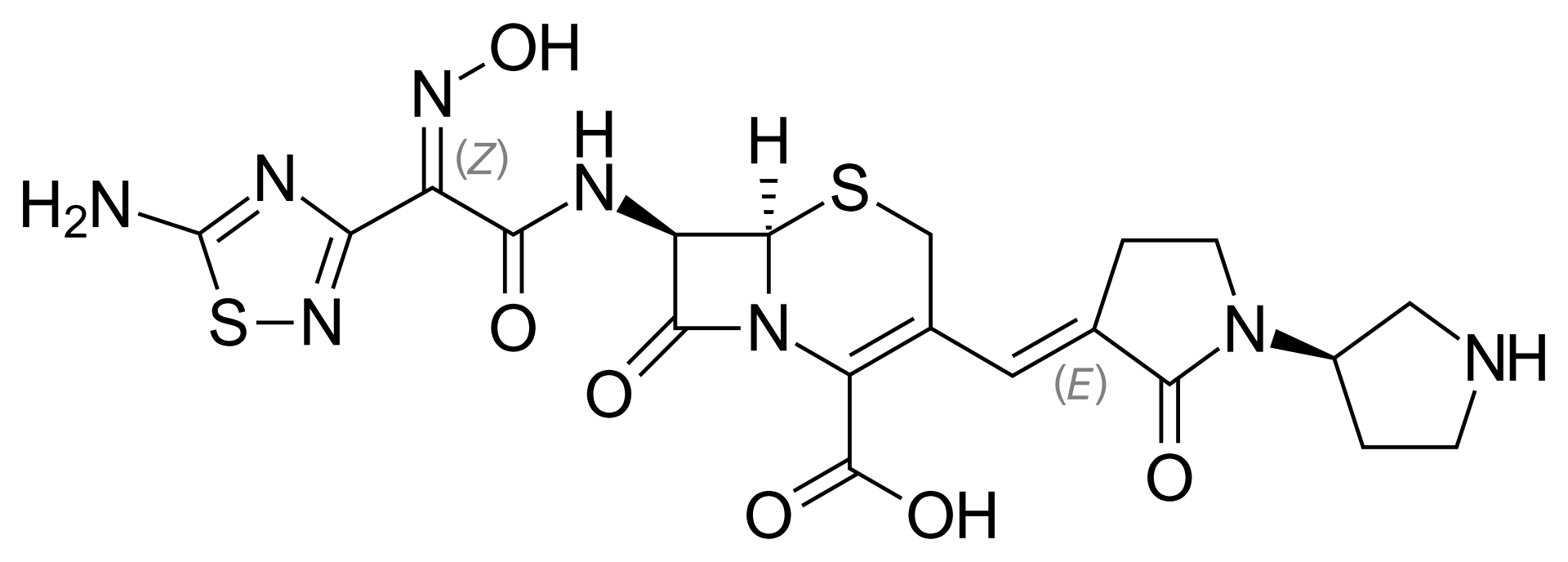
Препарат цефтобипрола медокарил натрия служит водорастворимым пролекарством антибиотика цефтобипрола и вводится внутривенно. В настоящее время он лицензирован в нескольких европейских странах и Канаде только для лечения пневмонии, в России - для лечения осложненных инфекций кожи и ее придатков, включая инфицированную диабетическую стопу без сопутствующего остеомиелита. В США показаниями для назначения препарата стали бактериемия, вызванная золотистым стафилококком (Staphylococcus aureus) у взрослых, в том числе с правосторонним инфекционным эндокардитом; острые бактериальные инфекции кожи и ее придатков у взрослых, а также внебольничная пневмония у взрослых и детей с трехмесячного возраста.
Поводом для решения FDA стали результаты трех клинических испытаний, в которых цефтобипрол сравнивали с даптомицином (при бактериемии), ванкомицином с азтреонамом (при кожных инфекциях) и стандартным цефалоспорином с возможностью добавления линезолида (при пневмонии у взрослых и детей). Во всех случаях антибиотик продемонстрировал эффективность по меньшей мере не худшую, чем препараты сравнения.
Автор: Олег Лищук
Ссылка на источник

Препарат цефтобипрола медокарил натрия служит водорастворимым пролекарством антибиотика цефтобипрола и вводится внутривенно. В настоящее время он лицензирован в нескольких европейских странах и Канаде только для лечения пневмонии, в России - для лечения осложненных инфекций кожи и ее придатков, включая инфицированную диабетическую стопу без сопутствующего остеомиелита. В США показаниями для назначения препарата стали бактериемия, вызванная золотистым стафилококком (Staphylococcus aureus) у взрослых, в том числе с правосторонним инфекционным эндокардитом; острые бактериальные инфекции кожи и ее придатков у взрослых, а также внебольничная пневмония у взрослых и детей с трехмесячного возраста.
Поводом для решения FDA стали результаты трех клинических испытаний, в которых цефтобипрол сравнивали с даптомицином (при бактериемии), ванкомицином с азтреонамом (при кожных инфекциях) и стандартным цефалоспорином с возможностью добавления линезолида (при пневмонии у взрослых и детей). Во всех случаях антибиотик продемонстрировал эффективность по меньшей мере не худшую, чем препараты сравнения.
Автор: Олег Лищук
Ссылка на источник